آخرین مطالب

در صورت پرخوری در شب یلدا، برای بدن خود اضافهکاری خریدهاید
پرخوری در یک شب، بدن را وارد وضعیت اضطراری میکند
پرخوری در یک شب، فقط یک خاطره سنگین یا دلدرد ساده نیست. بسیاری از ما تجربهاش را داریم؛ شبی که به دلایل مختلف مهمانی، استرس، شادی، خستگی یا حتی بیحوصلگی، بیش از نیاز بدن غذا میخوریم و با این تصور میخوابیم که فردا همه چیز درست میشود. اما علم میگوید بدن، حتی به یک شب پرخوری هم بیتفاوت نیست. در پشت صحنه، مجموعهای از واکنشهای پیچیده در دستگاه گوارش، هورمونها، مغز، قلب، کبد و حتی سیستم ایمنی آغاز میشود؛ واکنشهایی که گرچه اغلب موقتند، اما واقعی، قابل اندازهگیری و گاهی هشداردهندهاند.

چرا هنگام بارش برف، محیط ساکت میشود
برف با ساختار متخلخل خود، بازتاب صدا در فضا را محدود میکند
سکوت شهر در لحظات بارش برف، یکی از آشناترین و در عین حال مرموزترین تجربههای انسانی است. صداها عقب مینشینند، هیاهو محو میشود و فضا حالتی آرام و مهآلود به خود میگیرد. این سکوت نهتنها در روستاهای دورافتاده، بلکه حتی در قلب شلوغترین شهرها هم احساس میشود. اما این آرامش فقط یک حس شاعرانه نیست، پشت آن سازوکاری دقیق و علمی پنهان شدهاست. ترکیبی شگفتانگیز از فیزیک، هواشناسی، رفتار انسان و حتی روانشناسی مغز است.
نوع همانندسازی DNA با احتمال بروز سرطان مرتبط است
نحوه همانندسازی DNA در سلولهای بنیادی روده، عاملی پنهان اما تعیینکننده در شکلگیری یا پیشگیری از سرطان است. روده کوچک با بهکارگیری سازوکارهای حفاظتی در کپیبرداری از ماده ژنتیکی، خطاهای خطرناک را به حداقل میرساند، در حالیکه روده بزرگ با تکیه بر همانندسازی سریعتر و کماحتیاطتر، بستر مناسبی برای انباشت جهشهای سرطانی فراهم میکند؛ تفاوتی مولکولی که در نهایت به شکافی تا ۷۰ درصد در خطر ابتلا به سرطان میانجامد.

چرا بعضیها بعد از آرایش سردرد میگیرند؟
سردرد ریملی واقعیت پزشکی ندارد
اینبار سردرد پس از استفاده از یک برس کوچک ریمل شروع میشود. نه از کمخوابی، نه از استرس و نه حتی از نور صفحهنمایش. فقط چند دقیقه بعد از آرایش چشم، فشار آرامی پشت پیشانی یا شقیقهها شکل میگیرد؛ فشاری که کمکم تبدیل به درد میشود. تجربهای که بسیاری آن را با یک نام غیررسمی میشناسند: سردرد ریملی. اما آیا این درد واقعی است، یا فقط یک تصادف زمانی که بیدلیل به ریمل نسبت داده میشود؟

۵ مرحله خلاقیت نشان میدهد ژنِ ما حامل میلِ به خلق کردن است
خلاقیت در DNA انسان جریان دارد
تقریباً همه ما لحظهای را تجربه کردهایم که احساس میکنیم خلاقیت از ما فاصله گرفته است؛ انگار ذهن خاموش شده و هیچ ایدهای حاضر نیست سر برسد. روزی پر از کار، خستگی، ظرفهای نشسته و پیامهای ناتمام، و ناگهان این سؤال بیصدا در ذهن شکل میگیرد: «پس آن نیروی خلاق کجاست؟» علم روانشناسی امروز میگوید خلاقیت گم نشده؛ فقط در مرحلهای از مسیر طبیعی خود قرار دارد. مسیری که برخلاف تصور رایج، ناگهانی و جادویی نیست، بلکه روندی تدریجی، قابلپیشبینی و عمیقاً انسانی است.

ساعتی درون ماست که در حال خاموش شدن است
ماه، ساعت درونی بدن انسان را تنظیم میکند
پیش از آنکه برق شب را تسخیر کند، تاریکی هرگز کامل نبود. نور ماه، آرام و منظم، شبها را روشن میکرد و بیآنکه بدانیم، ریتم زندگی ما را تنظیم میساخت. خواب، بیداری، باروری و حتی احساس گذر زمان، همگی در هماهنگی با این چرخه ۲۹ روزه شکل میگرفتند. اما امروز، در جهانی غرق در نورهای مصنوعی، این نشانه کهن بهتدریج محو میشود. پژوهشهای تازه نشان میدهد انسانها هنوز یک «ساعت قمری درونی» دارند، اما نور شهرها، صفحهنمایشها و آسمان همیشهروشن، آن را از تنظیم خارج کرده است.

ژنها رازهای پنهان زندگی و مرگ بتهوون را آشکار کردند
موهای بتهوون زبان باز کردند. بتهوون پیش از مرگ، وصیتی عجیب بر جای گذاشت. او از برادرانش خواست که بیماریاش را پنهان نکنند و حقیقت را با مردم در میان بگذارند. او میخواست جهان بداند چه بر سر جسمش آمده است. نزدیک به دویست سال بعد، علم ژنتیک راهی پیدا کرد تا این وصیت را به شکلی تحققبخش انجام دهد که حتی خود بتهوون هم هرگز تصورش را نمیکرد.

اسکیزوفرنی نتیجه همزمان ژن و فشارهای محیطی است
اسکیزوفرنی ناگهان از راه نمیرسد؛ آرام، تدریجی و اغلب از جایی شروع میشود که نه دیده میشود و نه جدی گرفته میشود. این اختلال روانپزشکی مزمن، میتواند تفکر، ادراک، احساسات و رفتار فرد را بهگونهای تغییر دهد که مرز میان واقعیت و خیال برای او کمرنگ شود.
وقتی سلولها راه جایگزین پیدا میکنند
سلولها راه تازهای برای جبران یک بیماری ژنتیکی نادر پیدا میکنند
تشخیص یک بیماری ژنتیکی نادر برای دههها، اغلب به معنای پذیرش یک مسیر بیبازگشت بوده است؛ بیماریای که از کودکی آغاز میشود، بهتدریج توان حرکت و تعادل را میگیرد و در نهایت عمر را کوتاه میکند. اما کشف تازهای در زیستشناسی سلولی نشان میدهد حتی زمانی که یک پروتئین حیاتی در بدن غایب است، سلولها ممکن است راهی غیرمنتظره برای جبران پیدا کنند. پژوهش جدیدی اکنون امید واقعی برای بیماران مبتلا به «آتاکسی فریدریش» ایجاد کرده است.

ترکیبی در شکلات تلخ با نشانههای دیرتر پیر شدن پیوند میخورد
شکلات تلخ بخورید تا دیرتر پیر شوید
شاید برای بسیاری از ما شکلات تلخ تنها یک لذت کوچک روزانه باشد، اما پژوهش تازهای نشان میدهد که در دل این خوراکی محبوب، ترکیبی نهفته است که ممکن است با روند کندتر پیرشدن بدن ارتباط داشته باشد.

دورهمیهای غذایی، خوشحالی را در مغز فعال میکند
هیچکس بهتنهایی جشن نمیگیرد. از وعدههای خانوادگی گرفته تا مهمانیهای شلوغ، از عیدها تا جشنهای ساده دوستانه، غذا خوردن بهانهای است که انسانها را گرد یک میز میآورد و برای لحظهای کوتاه، جهان بیرون را پشت در نگه میدارد. عجیب است که عملی به ظاهر ساده مثل گذاشتن لقمهای در دهان چنین نیروی پیونددهندهای دارد. اما علم میگوید این تجربه، بسیار فراتر از رفع گرسنگی است. هر بار که کنار دیگران مینشینیم و لقمهای مشترک میخوریم، شبکههای عمیق ارتباطی در مغز فعال میشود؛ شبکههایی که از میلیونها سال پیش تا امروز، بقای ما را تضمین کردهاند.

مغز در خیالپردازی خود را بازسازی میکند
استراحت مغز، خیالپردازی است و این حالت نقش حیاتی در کارکرد مغز دارد. لحظههایی هست که نگاهمان روی نقطهای دور ثابت میماند و رشته افکارمان بیمحابا میان گذشته و آینده میلغزد. این لحظههای ظاهراً «بیکاری» همان زمانهایی هستند که مغز ما در سکوت، مشغول یکی از مهمترین فرایندهای زیستی خود است. خیالپردازی، که در نگاه اول شاید تنها پرسهزدن ذهن میان تصاویر و خاطرات باشد، در واقع سازوکاری پیچیده و ضروری برای سلامت ذهن انسان است.

دانشمندان دقیقترین تصویر را از درون قطرات DNA ثبت کردند
معجزهای از فشردهسازی مولکولی، در دل هر سلول انسان رخ میدهد. نزدیک به 2 متر DNA باید در فضایی جای بگیرد که تنها یکدهم قطر یک تار مو است و با وجود این تراکم عجیب، باید همیشه آماده خواندهشدن و فعالیتهای حیاتی باشد. اما تازهترین پژوهشها نشان میدهد که این نظم شگفتانگیز، تنها نتیجه فشردهسازی ساده نیست. گروهی از دانشمندان موفق شدهاند برای نخستینبار، دقیقترین تصاویر تاریخ را از درون قطرههای «کروماتین» ثبت کنند.
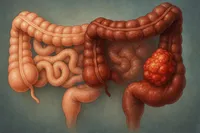
تفاوتهای سلولی دو روده مسیر سرطان را تغییر میدهند
چرا روده بزرگ بیشتر از روده کوچک سرطان میگیرد
روده کوچک، با طول خیرهکننده ۶ متری و میلیاردها سلول فعال، یکی از شلوغترین و پیچیدهترین بافتهای بدن انسان است؛ عضوی که هر روز مواد غذایی را تجزیه، جذب و پردازش میکند. در مقابل، روده بزرگ تنها یکونیم متر طول دارد، کارش سادهتر بهنظر میرسد و اغلب در انتهای زنجیره گوارش قرار گرفته است. با این حال یک معما وجود دارد: سرطان در روده بزرگ بسیار شایعتر است تا روده کوچک.

ورزشکاران به طور مرموزی در معرض ابتلا به آریتمی قلبی هستند
وقتی از سلامت قلب صحبت میکنیم، نخستین نسخهای که پزشکان و مربیان و پژوهشگران یکصدا تجویز میکنند، ورزش است. دویدن، شنا کردن، دوچرخهسواری، تمرینهای هوازی و هر چیزی که قلب را به حرکت وادارد، معمولاً بهعنوان بهترین دارو معرفی میشود. اما پشت این قاعده ساده، استثنایی حیرتانگیز پنهان است؛ استثنایی که سالهاست ذهن پزشکان ورزشی و فیزیولوژیستها را درگیر کرده. چرا برخی از سالمترین بدنهای دنیا، یعنی بدن ورزشکاران استقامتی، در معرض خطری قرار میگیرند که باید از آن دور باشند؟
آینده مردان در دستان یک ژن تازه رقم میخورد
تحول ژنتیکی، سرنوشت کروموزوم Y را تهدید میکند
«کروموزومY»زیر تیغ تکامل میرود. سرنوشت مردان، در نگاه بسیاری از زیستشناسان، درون مسیری باریک از DNA نوشته شده است؛ مسیری که شاید چند میلیون سال دیگر باقی نماند. کروموزوم Y، حامل راز تعیین جنسیت در انسان، امروز تنها سایهای از گذشته خود است؛ از ۸۰۰ ژن مشترک با «کروموزوم X»، حالا فقط نزدیک به ۳ درصد باقی مانده است. این کاهش طولانیمدت طی ۳۰۰ میلیون سال زیستشناسان را وامیدارد بپرسند که آیا این کروموزوم واقعاً در مسیر نابودی است؟ و اگر آری، آینده مرد بودن چگونه رقم خواهد خورد؟

کاهش رفتوآمد فشار روانی را کم میکند
دورکاری سلامت روان را دگرگون میکند
خانه جایی است که باید امنترین نقطه جهان باشد؛ فضایی که در آن بخشی از بار روز را زمین میگذاریم. اما حالا در دنیای پساکرونا، برای میلیونها نفر این «پناهگاه» به محل کار تبدیل شده است. این تغییر بزرگ نه یک تصمیم فردی، بلکه یک دگرگونی فرهنگی است که ساختار زندگی و سلامت روان ما را بازنویسی کرده است.

شیر فاقد هرگونه نقش مستقیم در فرآیند فیزیولوژیک سمزدایی بدن میباشد
سالهاست که با شدت گرفتن آلودگی هوا، توصیهای آشنا تکرار میشود: «شیر بخور تا سموم آلودگی از بدنت دفع شود.» این توصیه چنان رایج شده که گویی پشتوانهای قطعی دارد. با این حال، بررسیهای علمی نشان میدهد رابطه میان شیر و سمزدایی بسیار پیچیدهتر، محدودتر و دورتر از تصور رایج است؛ تا آنجا که بخش مهمی از این باور بیشتر ریشه در سنت و شایعات قدیمی دارد تا شواهد قطعی زیستپزشکی.

سوختوساز پنهانی که زمستان آن را بیدار میکند
بدن با کاهش دما چربی قهوهای را بهکار میاندازد
سرما همیشه حضوری ناخوانده در زندگی ما بوده است. این تجربه آشنا، هرچند ناخوشایند، کلیدی در دل خود دارد که میتواند سلامت و انرژی ما را دگرگون کند. پشت این لرزش کوتاه و هوای نفسگیر، لایهای از بافت بدن آرامآرام فعال میشود؛ «چربی قهوهای». بافتی کوچک، پنهان و کمحجم که برخلاف چربی سفید، نه باری بر دوش متابولیسم بلکه موتور کوچک گرماساز بدن است. سردی زمستان ممکن است مزاحم باشد، اما برای این چربی شگفتانگیز حکم دکمه روشنکنندهای را دارد که هر بار بدن سرد میشود، شعله آن بالا میرود. این گزارش روایتی است از اینکه چگونه سرمایی که از آن میگریزیم، شاید بتواند یکی از ابزارهای مهم سلامت ما باشد.

تعطیلات میل به غذا خوردن را تقویت میکند
تعطیلات فقط زمان استراحت نیست؛ زمان بیدار شدن اشتهایی است که انگار هفتهها منتظر یک بهانه بودهاست. بسیاری از ما در همان روزهای آغازین تعطیلی، متوجه میشویم که بیدلیل به سراغ یخچال میرویم، حجمهای بیشتری میخوریم یا بیآنکه گرسنه باشیم، با دیدن یک شیرینی یا بوی غذای خانگی تسلیم میشویم. این پدیده، برخلاف ظاهر سادهاش، نتیجه مجموعهای از تغییرات عصبی، هورمونی، روانشناختی و فرهنگی است؛ تغییراتی که بدن را وارد حالتی میکند که میل به غذا نهتنها طبیعی، بلکه تا حد زیادی قابل پیشبینی میشود.









